অধ্যায় - ৫
মৌলৰ পর্যাবৃত্ত শ্রেণীবিভাজন
MAIN CONTENT
প্ৰশ্নাৱলী :
১. নিউলেণ্ডছ অষ্টকৰ স্তম্ভবোৰত ড’বাৰেইনাৰৰ ট্ৰায়াড আছিলনে? তুলনা কৰা আৰু বিচাৰি উলিওৱা।
উত্তৰ: হয়, নিউলেণ্ডছৰ অষ্টকৰ স্তম্ভত ড’বাৰেইনাৰৰ ট্ৰায়াড আছিল । উদাহৰণস্বৰূপে, লিথিয়াম (Li), ছ’ডিয়াম (Na) আৰু পটেছিয়াম (K) - এই তিনিটা মৌল নিউলেণ্ডছৰ অষ্টক তালিকাৰ একেটা স্তম্ভতে পোৱা যায় , যিয়ে ড’বাৰেইনাৰৰ এটা ট্ৰায়াড গঠন কৰে ।
২. ড’বাৰেইনাৰৰ শ্ৰেণীবিভাজনৰ সীমাবদ্ধতাবোৰ কি কি আছিল ?
উত্তৰ: ড’বাৰেইনাৰৰ শ্ৰেণীবিভাজনৰ মূল সীমাবদ্ধতা আছিল যে তেওঁ সেই সময়লৈকে জ্ঞাত হোৱা সকলোবোৰ মৌলৰ পৰা মাত্ৰ তিনিটা ট্ৰায়াডহে চিনাক্ত কৰিব পাৰিছিল । সেইবাবে সকলো মৌলৰ বাবে এই পদ্ধতিটো ব্যৱহাৰোপযোগী নাছিল ।
৩. নিউলেণ্ডছৰ অষ্টক সূত্ৰৰ সীমাবদ্ধতাবোৰ কি কি আছিল ?
উত্তৰ: নিউলেণ্ডছৰ অষ্টক সূত্ৰৰ সীমাবদ্ধতাবোৰ হ’ল:
এই সূত্ৰটো কেৱল কেলছিয়াম পৰ্যন্তহে প্ৰযোজ্য আছিল ।
নিউলেণ্ডছে ধৰি লৈছিল যে প্ৰকৃতিত কেৱল ৫৬ টা মৌলহে আছে, কিন্তু পাছলৈ নতুন মৌল আৱিষ্কাৰ হোৱাত সেইবোৰ অষ্টক সূত্ৰত খাপ খোৱা নাছিল ।
একে ধৰ্ম নথকা কিছুমান মৌলকো (যেনে: ক'বাল্ট আৰু নিকেলক ফ্লু'ৰিন, ক্ল'ৰিনৰ সৈতে) একেটা স্তম্ভতে ৰখা হৈছিল ।
এই সূত্ৰটো কেৱল পাতল মৌলবোৰৰ ক্ষেত্ৰতহে ভালদৰে প্ৰযোজ্য হৈছিল ।
প্ৰশ্নাৱলী :
১. মেণ্ডেলিভৰ পৰ্য্যাবৃত্ত তালিকাখন ব্যৱহাৰ কৰি তলত দিয়া মৌলকেইটাৰ অক্সাইডৰ সংকেত নিৰ্ণয় কৰা।— K, C, Al, Si, Ba।
উত্তৰ: মেণ্ডেলিভৰ তালিকা অনুসৰি এই মৌলবোৰৰ অক্সাইডৰ সংকেত হ'ল:
K (পটেছিয়াম): 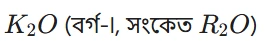
C (কাৰ্বন): 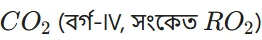
Al (এলুমিনিয়াম): 
Si (ছিলিকন): 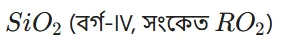
Ba (বেৰিয়াম): 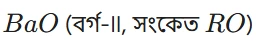
২. গেলিয়ামৰ উপৰিও আন কোনকেইটা মৌলৰ বাবে মৌলকেইটা আবিষ্কৃত হোৱাৰ পূৰ্বেই মেণ্ডেলিভে তেওঁৰ তালিকাত ঠাই ৰাখি থৈ গৈছিল? (যিকোনো দুটা)
উত্তৰ: মেণ্ডেলিভে গেলিয়ামৰ উপৰিও স্কেনডিয়াম (Sc) আৰু জাৰ্মেনিয়াম (Ge) মৌলৰ বাবে খালী ঠাই ৰাখি থৈ গৈছিল ।
৩. মেণ্ডেলিভে তেওঁৰ পৰ্য্যাবৃত্ত তালিকাখন যুগুতাওঁতে মানি চলা নীতিবোৰ (criteria) কি কি আছিল?
উত্তৰ: মেণ্ডেলিভে মানি চলা মূল নীতিবোৰ আছিল:
মৌলবোৰক সিহঁতৰ পাৰমাণৱিক ভৰৰ বৰ্দ্ধিত ক্ৰমত সজাইছিল I
একে ধৰণৰ ভৌতিক আৰু ৰাসায়নিক ধৰ্ম থকা মৌলবোৰক একেটা বৰ্গত স্থান দিছিল I
মৌলবোৰে অক্সিজেন আৰু হাইড্ৰ'জেনৰ সৈতে গঠন কৰা অক্সাইড আৰু হাইড্ৰাইডসমূহৰ সংকেতক মূল ৰাসায়নিক ধৰ্ম হিচাপে লৈছিল I
৪. সম্ভ্ৰান্ত গেছবোৰক এটা সুকীয়া বৰ্গত কিয় স্থান দিয়া হৈছে?
উত্তৰ: সম্ভ্ৰান্ত গেছবোৰ (যেনে- হিলিয়াম, নিয়ণ, আৰ্গন) অতিশয় নিষ্ক্ৰীয় আৰু আমাৰ বায়ুমণ্ডলত এইবোৰ নিচেই কম মাত্ৰাত থাকে । যিহেতু এইবোৰৰ ধৰ্ম আন মৌলতকৈ সম্পূৰ্ণ পৃথক, সেয়েহে পূৰ্বৰ ক্ৰমৰ কোনো সাল-সলনি নকৰাকৈ ইহঁতক এটা নতুন সুকীয়া বৰ্গত সহজে সংস্থাপিত কৰা হৈছিল ।
প্ৰশ্নাৱলী :
১. আধুনিক পৰ্য্যাবৃত্ত তালিকাই মেণ্ডেলিভৰ পৰ্য্যাবৃত্ত তালিকাত থকা আঁসোৱাহবোৰ কি দৰে দূৰ কৰিছিল?
উত্তৰ: আধুনিক পৰ্য্যাবৃত্ত তালিকায় পাৰমাণৱিক সংখ্যাক ভিত্তি হিচাপে লৈ মেণ্ডেলিভৰ আঁসোৱাহবোৰ তলত দিয়া ধৰণে দূৰ কৰে:
সমস্থানিকৰ স্থান: মৌলৰ সমস্থানিকবোৰৰ পাৰমাণৱিক সংখ্যা একে হোৱা বাবে সিহঁতক একেটা স্থানতে ৰখাৰ সমস্যা সমাধান হ'ল I
ক'বাল্ট আৰু নিকেলৰ স্থান: বেছি পাৰমাণৱিক ভৰৰ ক'বাল্টক (২৭) কম ভৰৰ নিকেলৰ (২৮) আগত ৰখাৰ বিসংগতি আঁতৰ হ'ল, কাৰণ ক'বাল্টৰ পাৰমাণৱিক সংখ্যা নিকেলতকৈ কম ।
হাইড্ৰ'জেনৰ অৱস্থান: হাইড্ৰ'জেনৰ স্থান সম্পৰ্কে থকা বিভ্ৰান্তি ইয়াৰ ইলেক্ট্ৰনীয় বিন্যাসৰ জৰিয়তে সঠিকভাৱে বুজিব পৰা গ'ল ।
২. মেগনেছিয়ামৰ দৰে ৰাসায়নিক বিক্ৰিয়া দেখুৱাব বুলি ভবা দুটা মৌলৰ নাম লিখা। তোমাৰ এই বাচনিৰ ভিত্তি কি?
উত্তৰ: মেগনেছিয়ামৰ দৰে ৰাসায়নিক ধৰ্ম দেখুওৱা দুটা মৌল হ’ল বেৰিলিয়াম (Be) আৰু কেলছিয়াম (Ca) । বাচনিৰ ভিত্তি: এই তিনিওটা মৌল আধুনিক পৰ্য্যাবৃত্ত তালিকাৰ একেটা বৰ্গতে (বৰ্গ-২) অৱস্থিত আৰু সিহঁতৰ বহিৰতম কক্ষত একে সংখ্যক (২ টা) যোজক ইলেক্ট্ৰন আছে ।
৩. নাম লিখা:
(a) বহিৰতম কক্ষত এটাকৈ ইলেক্ট্ৰন থকা তিনিটা মৌল I
উত্তৰ: লিথিয়াম (Li), ছডিয়াম (Na), পটেছিয়াম (K)।
(b) বহিৰতম কক্ষত দুটাকৈ ইলেক্ট্ৰন থকা দুটা মৌল I
উত্তৰ: মেগনেছিয়াম (Mg), কেলছিয়াম (Ca)।
(c) পৰিপূৰ্ণ বহিৰতম কক্ষ থকা তিনিটা মৌল I
উত্তৰ: হিলিয়াম (He), নিয়ন (Ne), আৰ্গন (Ar) I
৪. (a) লিথিয়াম, ছডিয়াম, পটেছিয়াম— এই আটাইকেইটা ধাতু। ইহঁতে পানীৰে সৈতে বিক্ৰিয়া কৰি হাইড্ৰ’জেন গেছ মুক্ত কৰে। এই মৌলকেইটাৰ পৰমাণুৰ কিবা সাদৃশ্য আছেনে?
উত্তৰ: হয়, এই তিনিওটা মৌলৰে পৰমাণুৰ বহিৰতম কক্ষত মাত্ৰ এটাকৈ যোজক ইলেক্ট্ৰন থাকে ।
(b) হিলিয়াম এটা নিষ্ক্ৰিয় গেছ আৰু নিয়নো এটা প্ৰায় নিষ্ক্ৰিয় গেছ। ইহঁতৰ পৰমাণুবোৰৰ মাজত কি মিল থকা দেখা যায়?
উত্তৰ: দুয়োটা মৌলৰে পৰমাণুৰ বহিৰতম কক্ষটো ইলেক্ট্ৰনেৰে সম্পূৰ্ণৰূপে পৰিপূৰ্ণ হৈ থাকে ।
৫. আধুনিক পৰ্য্যাবৃত্ত তালিকাত থকা প্ৰথম দহোটা মৌলৰ ভিতৰত কোনকেইটা ধাতু?
উত্তৰ: প্ৰথম দহোটা মৌলৰ ভিতৰত ধাতু কেইটা হ’ল: লিথিয়াম (Li) আৰু বেৰিলিয়াম (Be) ।
৬. পৰ্য্যাবৃত্ত তালিকাত স্থান বিবেচনা কৰি তলৰ মৌলকেইটাৰ কোনটো আটাইতকৈ বেছি ধাতৱধৰ্মী হ’ব বুলি অনুমান কৰিবা? Ga, Ge, As, Se, Be।
উত্তৰ: এই মৌলকেইটাৰ ভিতৰত বেৰিলিয়াম (Be) আটাইতকৈ বেছি ধাতৱধৰ্মী হ’ব । কাৰণ পৰ্য্যাবৃত্ত তালিকাৰ এটা পৰ্যায়ত বাঁওফালৰ পৰা সোঁফাললৈ গ’লে ধাতৱীয় ধৰ্ম কমি যায় আৰু যিহেতু Be তালিকাৰ একেবাৰে বাঁওফালে অৱস্থিত (বৰ্গ-২), সেয়েহে ইয়াৰ ধাতৱধৰ্ম সৰ্বাধিক ।
অনুশীলনীৰ প্ৰশ্নোত্তৰ :
১. পৰ্য্যাবৃত্ত তালিকাৰ পৰ্য্যায়বোৰত বাঁওফালৰ পৰা সোঁফাললৈ যাওঁতে ঘটা পৰিৱৰ্তনৰ প্ৰকৃতিৰ ওপৰত আগবঢ়োৱা তলৰ উক্তি সমূহৰ কোনটো উক্তি শুদ্ধ নহয়?
উত্তৰ: (c) পৰমাণুবোৰে সিহঁতৰ যোজক ইলেকট্ৰন অধিক সহজে হেৰুৱায় ।(কাৰণ: পৰ্যায় এটাত বাঁওফালৰ পৰা সোঁফাললৈ গ'লে নিউক্লীয় আধান বৃদ্ধি পায়, যাৰ ফলত ইলেকট্ৰন হেৰুৱাটো কঠিন হৈ পৰে ।)
২. মৌল X য়ে XCl2 সংকেতৰ ক্ল’ৰাইড গঠন কৰে। মৌল X তলৰ কোনটোৰে সৈতে একেটা বৰ্গতে থকাৰ সম্ভাৱনা সবাতোকৈ বেছি?
উত্তৰ: (b) Mg । (কাৰণ: XCl2 সংকেতৰ পৰা বুজা যায় যে X মৌলটোৰ যোজ্যতা ২। মেগনেছিয়ামৰ (Mg) যোজ্যতাও ২, সেয়েহে ই একেটা বৰ্গৰ হ’ব ।)
৩. কোনটো মৌলৰ আছে:
(a) ইলেকট্ৰনপূৰ্ণ দুটা কক্ষ?
উত্তৰ: নিয়ন (Ne) । (বিন্যাস: 2, 8)
(b) 2, 8, 2 ইলেকট্ৰনীয় বিন্যাস?
উত্তৰ: মেগনেছিয়াম (Mg) ।
(c) যোজক কক্ষত চাৰিটা ইলেকট্ৰনৰে সৈতে মুঠ তিনিটা কক্ষ?
উত্তৰ: ছিলিকন (Si) । (বিন্যাস: 2, 8, 4)
(d) যোজক কক্ষত তিনিটা ইলেকট্ৰনৰে সৈতে মুঠ দুটা কক্ষ?
উত্তৰ: ব’ৰন (B) । (বিন্যাস: 2, 3)
(e) দ্বিতীয় কক্ষত প্ৰথম কক্ষৰ দুগুণ ইলেকট্ৰন?
উত্তৰ: কাৰ্বন (C) । (প্ৰথম কক্ষত ২ টা আৰু দ্বিতীয় কক্ষত ৪ টা থাকে)
৪. (a) পৰ্য্যাবৃত্ত তালিকাত ব’ৰনৰ সৈতে একেটা স্তম্ভতে থকা মৌলবোৰৰ কি কি সাধাৰণ ধৰ্ম আছে?
উত্তৰ:
এই সকলোবোৰ মৌলৰ যোজক ইলেকট্ৰনৰ সংখ্যা ৩ ।
এই মৌলবোৰৰ যোজ্যতা ৩ ।
(b) পৰ্য্যাবৃত্ত তালিকাত ফ্ল’ৰিনৰ সৈতে একেটা স্তম্ভতে (বৰ্গ ১৭) থকা মৌলবোৰৰ কি কি সাধাৰণ ধৰ্ম আছে?
উত্তৰ:
এই মৌলবোৰৰ বহিঃস্থতম কক্ষত ৭ টাকৈ ইলেকট্ৰন থাকে ।
এইবোৰ অত্যন্ত বিদ্যুৎ ঋণাত্মক অধাতু আৰু ইহঁতে একক ঋণাত্মক আধানযুক্ত আয়ন গঠন কৰে ।
৫. এটা পৰমাণুৰ ইলেকট্ৰনীয় বিন্যাস হ’ল 2, 8, 7
a. এই মৌলটোৰ পাৰমাণৱিক সংখ্যা কি?
উত্তৰ: ১৭ । (ই হ’ল ক্ল’ৰিন) I
b. তলৰ মৌলবোৰৰ কোনটোৰে সৈতে ইয়াৰ ৰাসায়নিক সাদৃশ্য থাকিব? (বন্ধনীৰ ভিতৰত পাৰমাণৱিক সংখ্যাবোৰ দিয়া হৈছে) N (7), F (9), P (15), Ar (18)
উত্তৰ: F (9) । (কাৰণ: ফ্ল’ৰিনৰ বিন্যাস (2, 7) আৰু দিয়া মৌলটোৰ যোজক ইলেকট্ৰন একে ।)
৬. পৰ্য্যাবৃত্ত তালিকাত তিনিটা মৌল A, B আৰু C স্থানসমূহ তলত দেখুওৱা হৈছে।
| ১৬ বৰ্গ | ১৭ বৰ্গ |
| - | A |
| - | - |
| B | C |
(a) মৌল A ধাতুনে অধাতু?
উত্তৰ: অধাতু । (কাৰণ ই বৰ্গ ১৭ ত আছে)
(b) C মৌলটো A তকৈ বেছি সক্ৰিয়নে কম সক্ৰিয়?
উত্তৰ: কম সক্ৰিয় । (বৰ্গ এটাত তললৈ গ'লে অধাতুৰ সক্ৰিয়তা কমে)
(c) C মৌলটো আকাৰত B তকৈ ডাঙৰনে সৰু?
উত্তৰ: সৰু । (কাৰণ পৰ্যায় এটাত সোঁফাললৈ পাৰমাণৱিক ব্যাসাৰ্ধ কমে) I
(d) মৌল A এ কেনে ধৰণৰ আয়ন, কেটায়ন বা এনায়ন গঠন কৰিব?
উত্তৰ: এনায়ন (Anion) । (ই এটা ইলেকট্ৰন গ্ৰহণ কৰি ঋণাত্মক আয়ন গঠন কৰিব) I
৭. নাইট্ৰ’জেন (পাৰমাণৱিক সংখ্যা 7) আৰু ফছফ’ৰাছ (পাৰমাণৱিক সংখ্যা 15) পৰ্য্যাবৃত্ত তালিকাৰ বৰ্গ 15 ত থাকে। এই মৌল দুটাৰ ইলেকট্ৰনীয় বিন্যাস লিখা। ইহঁতৰ কোনটো বেছি বিদ্যুৎঋণাত্মক হ’ব আৰু কিয়?
উত্তৰ: নাইট্ৰ’জেনৰ বিন্যাস: 2, 5 আৰু ফছফ’ৰাছৰ বিন্যাস: 2, 8, 5 । ইয়াত , নাইট্ৰ’জেন বেছি বিদ্যুৎঋণাত্মক হ’ব । কাৰণ বৰ্গ এটাত ওপৰৰ পৰা তললৈ গ'লে কক্ষৰ সংখ্যা বৃদ্ধি পায় আৰু নিউক্লীয় আকৰ্ষণ কমি যায়, যাৰ ফলত বিদ্যুৎঋণাত্মকতা কমে ।
৮. পৰমাণু এটাৰ ইলেকট্ৰনীয় বিন্যাস আধুনিক পৰ্য্যাবৃত্ত তালিকাত তাৰ স্থানৰ সৈতে কিদৰে জড়িত হৈ আছে?
উত্তৰ: মৌল এটাৰ ইলেকট্ৰনীয় কক্ষৰ সংখ্যাই তাৰ পৰ্যায় সূচায় আৰু মৌলটোৰ বহিঃস্থতম কক্ষত থকা যোজক ইলেকট্ৰনৰ সংখ্যাই তাৰ বৰ্গ নিৰ্ধাৰণ কৰে ।
৯. আধুনিক পৰ্য্যাবৃত্ত তালিকাত কেলছিয়াম (পাৰমাণৱিক সংখ্যা 20) 12, 19, 21 আৰু 38 পাৰমাণৱিক সংখ্যা বিশিষ্ট মৌলকেইটাৰ দ্বাৰা পৰিবেষ্টিত হৈ আছে। এইকেইটাৰ কাৰ কাৰ ভৌতিক আৰু ৰাসায়নিক ধৰ্মসমূহ কেলছিয়ামৰ সৈতে মিলে?
উত্তৰ:পাৰমাণৱিক সংখ্যা 12 (Mg) আৰু 38 (Sr) যুক্ত মৌল দুটাৰ ধৰ্ম কেলছিয়ামৰ সৈতে মিলিব ।(কাৰণ: এই আটাইকেইটা মৌল আধুনিক পৰ্য্যাবৃত্ত তালিকাৰ বৰ্গ 2 ৰ অন্তৰ্ভুক্ত আৰু ইহঁতৰ যোজক ইলেকট্ৰন একে ।)
১০. মেণ্ডেলিভৰ পৰ্য্যাবৃত্ত তালিকা আৰু আধুনিক পৰ্য্যাবৃত্ত তালিকাৰ মৌলৰ শ্ৰেণীবিভাজন (arrangement) তুলনা কৰা।
উত্তৰ:
| ভিত্তি | মেণ্ডেলিভৰ পৰ্য্যাবৃত্ত তালিকা | আধুনিক পৰ্য্যাবৃত্ত তালিকা |
| ভিত্তি | মৌলবোৰক পাৰমাণৱিক ভৰৰ ওপৰত ভিত্তি কৰি সজোৱা হৈছে । | মৌলবোৰক পাৰমাণৱিক সংখ্যাৰ ওপৰত ভিত্তি কৰি সজোৱা হৈছে । |
| বিসংগতি | হাইড্ৰ’জেনৰ স্থান নিশ্চিত নাছিল । | হাইড্ৰ’জেনৰ স্থানৰ বিসংগতি বহুখিনি দূৰ হ’ল । |
| সমস্থানিক | সমস্থানিকৰ বাবে কোনো সুকীয়া স্থান নাছিল । | পাৰমাণৱিক সংখ্যাই ভিত্তি হোৱা বাবে সমস্থানিকৰ স্থানৰ সমস্যা সমাধান হ’ল । |
| বৰ্গ আৰু পৰ্যায় | ৮ টা বৰ্গ আৰু ৬ টা পৰ্যায় আছিল । | ১৮ টা বৰ্গ আৰু ৭ টা পৰ্যায় আছে । |
মৌলৰ পর্যাবৃত্ত শ্রেণীবিভাজন অধ্যায়ৰ ১০০ টা MCQ প্ৰশ্ন
গুৰুত্বপূৰ্ণ ২ নম্বৰীয়া প্ৰশ্ন আৰু উত্তৰ :
১. ড’বাৰেইনাৰৰ ট্ৰায়াড বুলিলে কি বুজা ?
উত্তৰ: ১৮১৭ চনত জাৰ্মান ৰসায়নবিদ ড’বাৰেইনাৰে একে ধৰ্মৰ মৌলবোৰক তিনিটাকৈ সদস্য থকা কিছুমান গোটত ভাগ কৰিছিল। এই গোটবোৰক ট্ৰায়াড বোলা হয়। তেওঁ দেখুৱাইছিল যে ট্ৰায়াড এটাৰ মৌল তিনিটাক পাৰমাণৱিক ভৰৰ বৰ্ধিত ক্ৰমত সজালে মাজৰ মৌলটোৰ পাৰমাণৱিক ভৰ আন দুটা মৌলৰ পাৰমাণৱিক ভৰৰ প্ৰায় গড় মানৰ সমান হয়।
২. নিউলেণ্ডছৰ অষ্টক সূত্ৰটো লিখা।
উত্তৰ: নিউলেণ্ডছৰ অষ্টক সূত্ৰ অনুসৰি, যদি মৌলবোৰক তেওঁলোকৰ পাৰমাণৱিক ভৰৰ বৰ্ধিত ক্ৰমত সজাই যোৱা হয়, তেন্তে প্ৰতিটো অষ্টম মৌলৰ ধৰ্ম প্ৰথমটো মৌলৰ ধৰ্মৰ সৈতে একে হয়। ইয়াক সংগীতৰ অষ্টকৰ (সা, ৰে, গা, মা, পা, ধা, নি) সৈতে তুলনা কৰা হয়।
৩. মেণ্ডেলিভৰ পৰ্যাবৃত্ত সূত্ৰটো লিখা।
উত্তৰ: মেণ্ডেলিভৰ পৰ্যাবৃত্ত সূত্ৰটো হ’ল— "মৌলবোৰৰ ভৌতিক আৰু ৰাসায়নিক ধৰ্মসমূহ ইহঁতৰ পাৰমাণৱিক ভৰৰ পৰ্যায়ক্ৰমে সলনি হয়।" অৰ্থাৎ মৌলসমূহক পাৰমাণৱিক ভৰৰ বৰ্ধিত ক্ৰমত সজালে নিৰ্দিষ্ট অন্তৰালত একে ধৰ্মৰ মৌলৰ পুনৰাবৃত্তি ঘটে।
৪. আধুনিক পৰ্যাবৃত্ত সূত্ৰটো কি ? ই মেণ্ডেলিভৰ সূত্ৰতকৈ কেনেকৈ পৃথক ?
উত্তৰ: আধুনিক পৰ্যাবৃত্ত সূত্ৰটো হ’ল— "মৌলবোৰৰ ধৰ্মসমূহ ইহঁতৰ পাৰমাণৱিক সংখ্যাৰ পৰ্যায়ক্ৰমে সলনি হয়।" মেণ্ডেলিভৰ সূত্ৰৰ মূল আধাৰ আছিল পাৰমাণৱিক ভৰ, কিন্তু আধুনিক সূত্ৰৰ মূল আধাৰ হ’ল পাৰমাণৱিক সংখ্যা।
৫. মেণ্ডেলিভে তেওঁৰ পৰ্যাবৃত্ত তালিকাত খালী ঠাই কিয় ৰাখিছিল ?
উত্তৰ: মেণ্ডেলিভে তেওঁৰ তালিকাত খালী ঠাইবোৰক আসোঁৱাহ বুলি ভবাৰ পৰিৱৰ্তে সেই সময়ত আৱিষ্কাৰ নোহোৱা কিছুমান মৌলৰ অস্তিত্বৰ ভৱিষ্যতবাণী হিচাপেহে গ্ৰহণ কৰিছিল। তেওঁ বিশ্বাস কৰিছিল যে ভৱিষ্যতে সেই খালী ঠাইবোৰ পূৰণ কৰিব পৰা মৌল আৱিষ্কাৰ হ’ব (যেনে: গেলিয়াম, জাৰ্মেনিয়াম)।
৬. সম্ভ্ৰান্ত গেছবোৰক কিয় এটা সুকীয়া বৰ্গত ৰখা হৈছে ?
উত্তৰ: সম্ভ্ৰান্ত গেছবোৰ (যেনে: হিলিয়াম, নিয়ন, আৰ্গন) অতিশয় নিষ্ক্ৰিয় আৰু ইহঁতৰ বহিৰতম কক্ষ ইলেকট্ৰনৰ দ্বাৰা সম্পূৰ্ণৰূপে ভৰ্তি হৈ থাকে। ইহঁতৰ ধৰ্ম আন মৌলতকৈ একেবাৰে পৃথক হোৱাৰ বাবে মূল তালিকাখনত ব্যাঘাত নজন্মোৱাকৈ ইহঁতক ১৮ নং বৰ্গত সুকীয়াকৈ ৰখা হৈছে।
৭. সমস্থানিক বা আইছ’টপবোৰে মেণ্ডেলিভৰ তালিকাৰ বাবে কেনেকৈ প্ৰত্যাহ্বানৰ সৃষ্টি কৰিছিল?
উত্তৰ: সমস্থানিকবোৰৰ ৰাসায়নিক ধৰ্ম একে কিন্তু পাৰমাণৱিক ভৰ বেলেগ বেলেগ। মেণ্ডেলিভৰ তালিকা পাৰমাণৱিক ভৰৰ ওপৰত ভিত্তি কৰি তৈয়াৰ কৰা হৈছিল, গতিকে একেটা মৌলৰে বিভিন্ন সমস্থানিকক তালিকাত ক’ত স্থান দিব লাগে, সেইটো এটা ডাঙৰ সমস্যা হৈ পৰিছিল।
৮. পৰ্যায় এটাত বাওঁফালৰ পৰা সোঁফাললৈ গ’লে পাৰমাণৱিক ব্যাসাৰ্ধ কিয় কমে ?
উত্তৰ: পৰ্যায় এটাত বাওঁফালৰ পৰা সোঁফাললৈ গ’লে পাৰমাণৱিক সংখ্যা বৃদ্ধি পায়, যাৰ ফলত কেন্দ্ৰৰ ধনাত্মক আধানৰ পৰিমাণ বাঢ়ে। এই বৃদ্ধি পোৱা আধানৰ প্ৰবল আকৰ্ষণৰ বাবে ইলেকট্ৰনবোৰ কেন্দ্ৰৰ ওচৰ চাপি আহে আৰু পৰমাণুৰ আকাৰ বা ব্যাসাৰ্ধ কমি যায়।
৯. বৰ্গ এটাৰ ওপৰৰ পৰা তললৈ গ’লে পাৰমাণৱিক আকাৰ কেনেকৈ সলনি হয় আৰু কিয় ?
উত্তৰ: বৰ্গ এটাৰ ওপৰৰ পৰা তললৈ গ’লে পাৰমাণৱিক আকাৰ বৃদ্ধি পায়। কাৰণ তললৈ যোৱাৰ লগে লগে একোটাকৈ নতুন ইলেকট্ৰনীয় কক্ষ (shell) যোগ হয়। যদিও কেন্দ্ৰীয় আধান বাঢ়ে, তথাপি নতুন কক্ষ যোগ হোৱাৰ ফলত কেন্দ্ৰৰ পৰা বহিৰতম কক্ষৰ দূৰত্ব বৃদ্ধি পায়।
১০. মৌলৰ যোজ্যতা কিহৰ ওপৰত নিৰ্ভৰ কৰে ? এটা উদাহৰণ দিয়া।
উত্তৰ: মৌল এটাৰ যোজ্যতা ইয়াৰ পৰমাণুৰ বহিৰতম কক্ষত থকা যোজক ইলেকট্ৰনৰ সংখ্যাৰ ওপৰত নিৰ্ভৰ কৰে। উদাহৰণস্বৰূপ, মেগনেছিয়ামৰ (Mg) পাৰমাণৱিক সংখ্যা ১২ আৰু ইয়াৰ ইলেকট্ৰনীয় বিন্যাস হ’ল ২, ৮, ২। যিহেতু ইয়াৰ বহিৰতম কক্ষত ২টা ইলেকট্ৰন আছে, গতিকে ইয়াৰ যোজ্যতা হ’ব ২।
১১. ধাতুকল্প কাক বোলে ? দুটা উদাহৰণ দিয়া।
উত্তৰ: যিবোৰ মৌলে ধাতু আৰু অধাতু— দুয়োৰে ধৰ্ম প্ৰদৰ্শন কৰে, সেইবোৰক ধাতুকল্প বা অৰ্ধধাতু (Metalloids) বোলে। আধুনিক পৰ্যাবৃত্ত তালিকাত এটা টেঁৰা-বেঁকা ৰেখাই ধাতু আৰু অধাতুবোৰক পৃথক কৰে আৰু এই ৰেখাৰ ওপৰত থকা মৌলবোৰেই হ’ল ধাতুকল্প। উদাহৰণ: চিলিকন (Si) আৰু জাৰ্মেনিয়াম (Ge)।
১২. মেণ্ডেলিভৰ পৰ্যাবৃত্ত তালিকাৰ দুটা আসোঁৱাহ লিখা।
উত্তৰ: মেণ্ডেলিভৰ তালিকাৰ দুটা আসোঁৱাহ হ’ল—
(i) হাইড্ৰ’জেনৰ স্থান নিৰ্দিষ্ট নাছিল, কাৰণ ই ক্ষাৰ ধাতু আৰু হেল’জেন দুয়োৰে সৈতে সাদৃশ্য দেখুৱাইছিল।
(ii) পাৰমাণৱিক ভৰৰ বৃদ্ধি সদায় সুষম নাছিল, যাৰ ফলত এটা মৌলৰ পিছত আনটো মৌল কি হ’ব সেইটো নিৰ্ণয় কৰা কঠিন আছিল।
১৩. যোজক ইলেকট্ৰন বুলিলে কি বুজা ? বৰ্গ এটাত ইয়াৰ কেনে পৰিৱৰ্তন হয় ?
উত্তৰ: পৰমাণু এটাৰ আটাইতকৈ বাহিৰৰ কক্ষত থকা ইলেকট্ৰনবোৰক যোজক ইলেকট্ৰন বোলে। একেটা বৰ্গত থকা সকলো মৌলৰ যোজক ইলেকট্ৰনৰ সংখ্যা সদায় একে থাকে। উদাহৰণস্বৰূপ, ১ নং বৰ্গৰ লিথিয়াম, ছডিয়াম আৰু পটেছিয়াম আটাইৰে যোজক ইলেকট্ৰনৰ সংখ্যা ১।
১৪. মেণ্ডেলিভে মৌলৰ শ্ৰেণীবিভাজনৰ বাবে অক্সিজেন আৰু হাইড্ৰ’জেনক কিয় বাচি লৈছিল ?
উত্তৰ: অক্সিজেন আৰু হাইড্ৰ’জেন অতি সক্ৰিয় মৌল আৰু ইহঁতে প্ৰায়বোৰ মৌলৰ সৈতে বিক্ৰিয়া কৰি অক্সাইড আৰু হাইড্ৰাইড গঠন কৰে। মেণ্ডেলিভে এই যৌগবোৰৰ ধৰ্মৰ ওপৰত ভিত্তি কৰি মৌলবোৰৰ শ্ৰেণীবিভাজন কৰিবলৈ সহজ হ’ব বুলি ভাবিছিল।
১৫. ইলেকট্ৰন ত্যাগ কৰাৰ প্ৰৱণতা কেনেকৈ সলনি হয়— (ক) পৰ্যায়ত (খ) বৰ্গত ?
উত্তৰ: (ক) পৰ্যায় এটাত বাওঁফালৰ পৰা সোঁফাললৈ গ’লে কাৰ্যকৰী কেন্দ্ৰীয় আধান বৃদ্ধি পায়, যাৰ ফলত ইলেকট্ৰন ত্যাগ কৰাৰ প্ৰৱণতা কমি যায়।
(খ) বৰ্গ এটাত ওপৰৰ পৰা তললৈ গ’লে বহিৰতম কক্ষৰ দূৰত্ব বৃদ্ধি পোৱাৰ বাবে কেন্দ্ৰৰ আকৰ্ষণ কমি যায় আৰু ইলেকট্ৰন ত্যাগ কৰা সহজ হয়।
১৬. অধাতুবোৰ কিয় বিদ্যুত ঋণাত্মক ?
উত্তৰ: অধাতুবোৰে সাধাৰণতে সিহঁতৰ বহিৰতম কক্ষ সম্পূৰ্ণ কৰিবলৈ ইলেকট্ৰন গ্ৰহণ কৰে। যিহেতু ইলেকট্ৰন গ্ৰহণ কৰিলে ঋণাত্মক আধান লাভ কৰে, সেইবাবে অধাতুবোৰক বিদ্যুত ঋণাত্মক মৌল বুলি কোৱা হয়।
১৭. আধুনিক পৰ্যাবৃত্ত তালিকাই মেণ্ডেলিভৰ তালিকাৰ আসোঁৱাহবোৰ কেনেকৈ দূৰ কৰিলে ?
উত্তৰ: আধুনিক পৰ্যাবৃত্ত তালিকাত পাৰমাণৱিক সংখ্যাক মূল আধাৰ হিচাপে লোৱা বাবে সমস্থানিকৰ সমস্যা সমাধান হ’ল (কাৰণ একেটা মৌলৰ সকলো সমস্থানিকৰ পাৰমাণৱিক সংখ্যা একে)। লগতে, মৌলসমূহক সিহঁতৰ ইলেকট্ৰনীয় বিন্যাসৰ ওপৰত ভিত্তি কৰি সজোৱা বাবে অসংগত স্থানবোৰৰো অন্ত পৰিল।
১৮. মেণ্ডেলিভৰ ‘একা-ব’ৰন’ আৰু ‘একা-এলুমিনিয়াম’ৰ বৰ্তমান নাম কি ?
উত্তৰ: মেণ্ডেলিভে ভৱিষ্যতবাণী কৰা ‘একা-ব’ৰন’ৰ বৰ্তমান নাম হ’ল স্কেনডিয়াম (Sc) আৰু ‘একা-এলুমিনিয়াম’ৰ বৰ্তমান নাম হ’ল গেলিয়াম (Ga)।
১৯. কক্ষ একোটাত ইলেকট্ৰনৰ বিতৰণ কোনটো সূত্ৰই নিৰ্ণয় কৰে? ৩য় কক্ষত সৰ্বাধিক কিমান ইলেকট্ৰন থাকে ?
উত্তৰ: কক্ষ একোটাত ইলেকট্ৰনৰ সৰ্বাধিক সংখ্যা $2n^2$ সূত্ৰৰ দ্বাৰা নিৰ্ণয় কৰা হয়, য’ত ‘n’ হ’ল কক্ষৰ ক্ৰমিক সংখ্যা। ৩য় কক্ষৰ (M কক্ষ) বাবে n = 3, গতিকে সৰ্বাধিক ইলেকট্ৰনৰ সংখ্যা হ’ব $2 \times 3^2 = 18$ টা।
২০. অক্সাইডৰ প্ৰকৃতি কেনেকৈ সলনি হয় ?
উত্তৰ: সাধাৰণতে ধাতুৰ অক্সাইডবোৰ ক্ষাৰকীয় প্ৰকৃতিৰ হয় আৰু অধাতুৰ অক্সাইডবোৰ আম্লিক প্ৰকৃতিৰ হয়। পৰ্যায় এটাত বাওঁফালৰ পৰা সোঁফাললৈ গ’লে মৌলবোৰৰ অক্সাইডৰ ধৰ্ম ক্ষাৰকীয়ৰ পৰা ক্ৰমান্বয়ে আম্লিকলৈ পৰিৱৰ্তিত হয়।