অধ্যায়ঃ ৩
ধাতু আৰু অধাতু
MAIN CONTENT
প্ৰশ্নাবলী :
১. ধাতু একোটাৰ উদাহৰণ দিয়া যি ধাতু—
(i) সাধাৰণ উষ্ণতাত (room temperature) জুলীয়া।
উত্তৰ: পাৰা (Mercury).
(ii) কটাৰীৰে সহজে কাটিব পাৰি।
উত্তৰ: ছ'ডিয়াম বা পটাছিয়াম.
(iii) তাপৰ আটাইতকৈ সুপৰিবাহী।
উত্তৰ: ৰূপ (Silver).
(iv) তাপৰ কম পৰিবাহী।
উত্তৰ: সীহ (Lead) বা পাৰা.
২. ধাতুৰ ঘাত সহনীয়তা আৰু নমনীয়তাৰ অৰ্থ বহলাই আলোচনা কৰা।
উত্তৰঃ ঘাত সহনীয়তা (Malleability): কিছুমান ধাতুক হাতুৰিৰে মৰিয়াই পিটি পাতল পাত এচটা বনাব পাৰি। ধাতুৰ এই ধৰ্মক ঘাতসহনীয়তা বোলে। উদাহৰণস্বৰূপে, সোণ আৰু ৰূপ আটাইতকৈ ঘাত সহনশীল ধাতু।
নমনীয়তা (Ductility): ধাতুৰ পাত দীঘল কৰি তাঁৰলৈ পৰিৱৰ্তন কৰিব পৰা গুণকে নমনীয়তা বোলে। সোণ আটাইতকৈ নমনীয় ধাতু; এক গ্ৰাম সোণৰ পৰা প্ৰায় দুই কিলোমিটাৰ দৈৰ্ঘ্যৰ তাঁৰ পাব পাৰি।
প্ৰশ্নাবলী :
১. ছডিয়াম ধাতু কিয় কেৰাচিন তেলত ডুবাই ৰখা হয়?
উত্তৰ: ছ'ডিয়াম ইমান সক্ৰিয় যে ই মুক্ত বায়ুত থকা অক্সিজেনৰ সৈতে অতি প্ৰৱণতাৰে বিক্ৰিয়া কৰে আৰু জুই জ্বলি উঠে। এই দুৰ্ঘটনা ৰোধ কৰিবলৈ আৰু বায়ুৰ অক্সিজেনৰ সংস্পৰ্শৰ পৰা আঁতৰাই ৰাখিবলৈ ইয়াক কেৰাচিন তেলত ডুবাই ৰখা হয়।
২. তলৰ বিক্ৰিয়াবিলাকৰ ৰাসায়নিক সমীকৰণ লিখা—
(i) উত্তপ্ত জলীয় বাষ্পৰ লগত আইৰনৰ বিক্ৰিয়া:
উত্তৰঃ 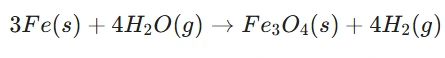
(ii) পানীৰ লগত কেলছিয়াম আৰু পটাছিয়ামৰ বিক্ৰিয়া:
উত্তৰঃ
কেলছিয়াম: 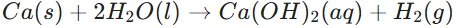
পটাছিয়াম: 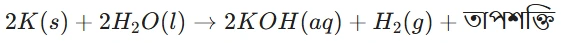
৩. A, B, C, D চাৰিটা ধাতু লৈ তলৰ দ্ৰৱণ বিলাকত এটা এটাকৈ দিয়া হৈছিল। ফলাফলবিলাক তলৰ তালিকাত লিপিবদ্ধ কৰা হৈছে।
| ধাতু | আইৰন(II) ছালফেট | কপাৰ (II) ছালফেট | জিংক ছালফেট | ছিলভাৰ নাইট্ৰেট |
| A | বিক্ৰিয়া নহয় | প্ৰতিস্থাপন | ||
| B | প্ৰতিস্থাপন | বিক্ৰিয়া নহয় | ||
| C | বিক্ৰিয়া নহয় | বিক্ৰিয়া নহয় | বিক্ৰিয়া নহয় | প্ৰতিস্থাপন |
| D | বিক্ৰিয়া নহয় | বিক্ৰিয়া নহয় | বিক্ৰিয়া নহয় | বিক্ৰিয়া নহয় |
ওপৰৰ তালিকা ব্যৱহাৰ কৰি A B C D ধাতু সম্বন্ধে তলৰ প্ৰশ্নবিলাকৰ উত্তৰ দিয়া।
(i) আটাইতকৈ সক্ৰিয় ধাতু কোনটো?
উত্তৰ: ধাতু B (কাৰণ ই আইৰনক তাৰ লৱণৰ পৰা অপসাৰিত কৰিব পাৰে)।
(ii) কপাৰ (II) ছালফেট লৱণত B ধাতু দিলে কি হ’ব?
উত্তৰ: প্ৰতিস্থাপন বিক্ৰিয়া ঘটিব, অৰ্থাৎ B ধাতুৱে কপাৰক অপসাৰিত কৰিব।
(iii) A, B, C, D ধাতুক সক্ৰিয়তাৰ নিম্নক্ৰমত সজোৱা:
উত্তৰঃ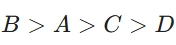
৪. লঘু হাইড্ৰ’ক্ল’ৰিক এছিডত (HCl) এটা সক্ৰিয় ধাতু দিলে কি গেছ উৎপন্ন হয়? আইৰনে লঘু H2SO4 ৰ লগত কৰা বিক্ৰিয়াটোৰ সমীকৰণ লিখা।
উত্তৰ: হাইড্ৰ’জেন গেছ (H2) উৎপন্ন হয়।
সমীকৰণ: 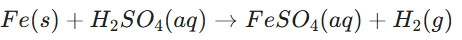
৫. আইৰন (II) ছালফেট দ্ৰৱণত জিংক ধাতু দিলে কি দেখিবা? সংঘটিত হোৱা বিক্ৰিয়াটো লিখা।
উত্তৰ: যিহেতু জিংক আইৰনতকৈ অধিক সক্ৰিয়, সেয়েহে ই আইৰন (II) ছালফেটৰ পৰা আইৰনক প্ৰতিষ্ঠাপিত কৰিব। দ্ৰৱণটোৰ ৰং সলনি হ’ব।
সমীকৰণ: 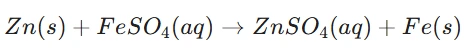
প্ৰশ্নাবলী :
(i) ছডিয়াম, অক্সিজেন আৰু মেগনেছিয়ামৰ ইলেক্ট্ৰন বিন্দু গঠন (electron dot structure) লিখা।
উত্তৰঃ ইলেক্ট্ৰন বিন্দু গঠন:
ছডিয়াম (Na): Na
অক্সিজেন (O): (৬ টা বিন্দুসহ O)
মেগনেছিয়াম (Mg): Mg
(ii) ইলেক্ট্ৰন স্থানান্তৰৰ জৰিয়তে Na2O আৰু MgO ৰ গঠন লিখা।
উত্তৰঃ
Na2O (ছডিয়াম অক্সাইড)ৰ গঠন : ছডিয়ামৰ পাৰমাণৱিক সংখ্যা ১১ আৰু ইয়াৰ ইলেক্ট্ৰনীয় বিন্যাস হ’ল ২, ৮, ১ । সুস্থিৰ অষ্টক বিন্যাস লাভ কৰিবলৈ ই বহিৰতম কক্ষৰ ১ টা ইলেক্ট্ৰন ত্যাগ কৰি ছডিয়াম কেটায়ন Na+ গঠন কৰে ।
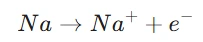
অক্সিজেন (O): অক্সিজেনৰ পাৰমাণৱিক সংখ্যা ৮ আৰু ইয়াৰ ইলেক্ট্ৰনীয় বিন্যাস হ’ল ২, ৬ । সুস্থিৰতাৰ বাবে ইয়াৰ ২ টা ইলেক্ট্ৰনৰ প্ৰয়োজন হয় ।
স্থানান্তৰ: ইয়াত দুটা ছডিয়াম পৰমাণুৱে এটাকৈ (মুঠ ২ টা) ইলেক্ট্ৰন ত্যাগ কৰে আৰু এটা অক্সিজেন পৰমাণুৱে সেই ২ টা ইলেক্ট্ৰন গ্ৰহণ কৰি অক্সাইড এনায়ন (O2-) গঠন কৰে ।
গঠন: এই বিপৰীত আধানযুক্ত আয়নসমূহ Na+ আৰু O2-প্ৰবল বিদ্যুৎ আকৰ্ষণী বলৰ দ্বাৰা বান্ধ খাই Na2O গঠন কৰে ।
MgO (মেগনেছিয়াম অক্সাইড)ৰ গঠন : মেগনেছিয়ামৰ পাৰমাণৱিক সংখ্যা ১২ আৰু ইয়াৰ ইলেক্ট্ৰনীয় বিন্যাস হ’ল ২, ৮, ২ । ই বহিৰতম কক্ষৰ ২ টা ইলেক্ট্ৰন ত্যাগ কৰি মেগনেছিয়াম কেটায়ন (Mg2+) গঠন কৰে ।
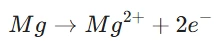
অক্সিজেন (O): অক্সিজেনৰ ইলেক্ট্ৰনীয় বিন্যাস হ’ল ২, ৬ । ইয়াক অষ্টক পূৰণ কৰিবলৈ ২ টা ইলেক্ট্ৰনৰ প্ৰয়োজন ।
স্থানান্তৰ: মেগনেছিয়াম পৰমাণুৱে ত্যাগ কৰা ২ টা ইলেক্ট্ৰন অক্সিজেন পৰমাণুটোৱে গ্ৰহণ কৰে আৰু অক্সাইড এনায়ন (O2-) লৈ পৰিণত হয় ।
গঠন: Mg2+ আৰু O2- আয়ন দুটাৰ মাজত থকা প্ৰবল বিদ্যুৎস্থিতীয় আকৰ্ষণ বলৰ ফলত MgO যৌগটো গঠিত হয় ।
(iii) এই যৌগটোত থকা আয়নসমূহ কি কি?
উত্তৰঃ এই যৌগটোত থকা আয়নসমূহ -

2. আয়নীয় যৌগৰ গলনাংক কিয় বেছি?
উত্তৰঃ আয়নীয় যৌগৰ গলনাংক বেছি কাৰণ বিপৰীত আধানযুক্ত আয়নবোৰৰ মাজৰ আন্তঃ আয়নীয় বিদ্যুৎস্থিতীয় আকৰ্ষণ বল অতি প্ৰবল। এই প্ৰবল বল ভাঙিবলৈ যথেষ্ট পৰিমাণৰ তাপশক্তিৰ প্ৰয়োজন হয়।
প্ৰশ্নাবলী :
1.তলত দিয়াবোৰৰ সংজ্ঞা লিখা।
(i) খনিজ (mineral)
উত্তৰঃভূত্বকত প্ৰাকৃতিকভাৱে পোৱা মৌল বা যৌগবোৰক খনিজ পদাৰ্থ বোলে।
(ii) আকৰ (ore)
উত্তৰঃযিবোৰ খনিজ পদাৰ্থৰ পৰা ধাতুবিধ লাভজনকভাৱে আহৰণ কৰিব পাৰি, সেইবোৰক আকৰ বোলে।
(iii) খনিজ মল (gangue)
উত্তৰঃআকৰৰ লগত মিহলি হৈ থকা বালি, মাটি আদি অশুদ্ধিবোৰক খনিজ মল বোলে।
2. প্ৰকৃতিত মুক্ত অৱস্থাত পোৱা দুটা ধাতুৰ নাম লিখা।
উত্তৰঃপ্ৰকৃতিত মুক্ত অৱস্থাত পোৱা দুটা ধাতুৰ নাম - সোণ (Gold) আৰু ৰূপ (Silver)।
3. অক্সাইডৰ পৰা ধাতু উৎপন্ন কৰিবলৈ কি ৰাসায়নিক পদ্ধতি প্ৰয়োগ কৰা হয়?
উত্তৰঃঅক্সাইডৰ পৰা ধাতু উৎপন্ন কৰিবলৈ বিজাৰণ (Reduction) ৰাসায়নিক পদ্ধতি প্ৰয়োগ কৰা হয় I
প্ৰশ্নাবলী :
1.জিংক, মেগনেছিয়াম আৰু কপাৰৰ ধাতুৰ অক্সাইড তলত দিয়া ধাতুবোৰৰ লগত উত্তপ্ত কৰা হ’ল।
| ধাতু | জিংক | মেগনেছিয়াম | কপাৰ |
| জিংক অক্সাইড | |||
| মেগনেছিয়াম অক্সাইড | |||
| কপাৰ অক্সাইড |
উত্তৰঃ
যিংক অক্সাইড + মেগনেছিয়াম → প্ৰতিস্থাপন ঘটিব।
কপাৰ অক্সাইড + জিংক → প্ৰতিস্থাপন ঘটিব।
কপাৰ অক্সাইড + মেগনেছিয়াম → প্ৰতিস্থাপন ঘটিব।
কোনবিলাক ক্ষেত্ৰত প্ৰতিস্থাপন বিক্ৰিয়া ঘটিব?
2. কোনবোৰ ধাতু সহজে ক্ষয় নহয়?
উত্তৰঃসক্ৰিয়তা শ্ৰেণীৰ একেবাৰে তলত থকা ধাতুসমূহ, যেনে সোণ আৰু প্লেটিনাম সহজে ক্ষয় নহয়।
3. সংকৰ ধাতু কি?
উত্তৰঃ সংকৰ ধাতু হ’ল দুটা বা ততোধিক ধাতু অথবা এটা ধাতু আৰু এটা অধাতুৰ সমসত্ব মিশ্ৰণ। যেনে— পিতল (কপাৰ আৰু যিংকৰ মিশ্ৰণ)।
অনুশীলনী :
1.তলৰ কোনবোৰ ক্ষেত্ৰত প্রতিস্থাপন বিক্রিয়া ঘটিব?
(a) NaCl ৰ দ্ৰৱ আৰু কপাৰ ধাতু।
(b) MgCl2 ৰ দ্ৰৱ আৰু এলুমিনিয়াম ধাতু।
(c) FeSO4 দ্ৰৱ আৰু ছিলভাৰ ধাতু।
(d) AgNO3 ৰ দ্ৰৱ আৰু কপাৰ ধাতু।
উত্তৰঃ (d) AgNO3 ৰ দ্ৰৱ আৰু কপাৰ ধাতু।
2. লোৰ টাৱা (iron frying pan) এখন মামৰে ধৰাৰ পৰা বচাই ৰাখিবলৈ তলৰ কোনটো পদ্ধতি উপযুক্ত হব?
(a) গ্রীজ ব্যৱহাৰ কৰি
(b) ৰং ব্যৱহাৰ কৰি
(c) যিংকৰ প্ৰলেপ দি
(d) ওপৰৰ সকলো
উত্তৰঃ (c) যিংকৰ প্ৰলেপ দি
3. এটা মৌলই অক্সিজেনৰ লগত বিক্রিয়া কৰি উচ্চ গলনাংকৰ যৌগ উৎপন্ন কৰে। যৌগটো পানীত দ্ৰৱণীয়। সম্ভৱপৰ মৌলটো— (a) কেলছিয়াম
(b) কার্বন
(c) ছিলিকন
(d) আইৰন
উত্তৰঃ(a) কেলছিয়াম
4. খাদ্যবস্তু ভৰাই ৰখা পাত্ৰবোৰত টিনৰ প্ৰলেপ দিয়া হয়; যিংকৰ নহয়। কিয়নো—
(a) টিনতকৈ যিংক দামী।
(b) যিংকৰ গলনাংক টিনতকৈ বেছি।
(c) যিংক টিনতকৈ অধিক সক্রিয়।
(d) যিংক টিনতকৈ কম সক্রিয়।
উত্তৰঃ(c) যিংক টিনতকৈ অধিক সক্ৰিয়।
কাৰণ: যিংক অধিক সক্ৰিয় হোৱা বাবে ই খাদ্যত থকা এছিডৰ লগত বিক্ৰিয়া কৰি বিষক্ৰিয়া সৃষ্টি কৰিব পাৰে ।
5. তোমাক এটা হাতুৰী, এটা বেটাৰী, অলপ তাঁৰ আৰু এটা ছুইচ দিয়া হ'ল।
(a) এই বস্তুবোৰ ব্যৱহাৰ কৰি ধাতু আৰু অধাতু কেনেকৈ চিনাক্ত কৰিবা?
উত্তৰঃ
হাতুৰীৰে: হাতুৰীৰে পিটিলে যদি পাতল পাতলৈ ৰূপান্তৰিত হয়, তেন্তে সেয়া ধাতু (ঘাতসহনীয়তা গুণৰ বাবে)। যদি ভাঙি টুকুৰা-টুকুৰ হয়, তেন্তে সেয়া অধাতু ।
বৈদ্যুতিক বৰ্তনীৰে: বেটাৰী, তাঁৰ, বাল্ব আৰু ছুইচেৰে এটা বৰ্তনী সাজি মৌলটো সংযোগ কৰিলে যদি বাল্বটো জ্বলি উঠে, তেন্তে সেয়া ধাতু (বিদ্যুতৰ সুপৰিবাহী বাবে) ।
(b) ধাতু/অধাতুৰ চিনাক্তকৰণত এই পৰীক্ষাবোৰৰ উপযোগিতা মূল্যাঙ্কন কৰা।
উত্তৰঃএই পৰীক্ষাবোৰে মৌলৰ ভৌতিক ধৰ্মৰ পাৰ্থক্য স্পষ্ট কৰে। অৱশ্যে কেৱল ভৌতিক ধৰ্মৰ ওপৰত ভিত্তি কৰি শ্ৰেণীবিভাগ কৰিলে কিছু ব্যতিক্ৰম থাকিব পাৰে (যেনে- গ্ৰেফাইট অধাতু হ’লেও বিদ্যুতৰ পৰিবাহী) ।
6. উভধর্মী অক্সাইড কাক বোলে? দুটা উভধর্মী অক্সাইডৰ উদাহৰণ দিয়া।
উত্তৰঃযিবোৰ ধাতৱ অক্সাইডে অম্ল (Acid) আৰু ক্ষাৰ (Base) উভয়ৰে লগত বিক্ৰিয়া কৰি লৱণ আৰু পানী উৎপন্ন কৰে, তাক উভধৰ্মী অক্সাইড বোলে ।
উদাহৰণ: এলুমিনিয়াম অক্সাইড (Al2O3) আৰু যিংক অক্সাইড (ZnO) ।
7. দুটাকৈ ধাতুৰ নাম লিখা যিয়ে লঘু এছিডৰ পৰা হাইড্ৰ'জেন অপসাৰণ কৰে আৰু যিয়ে নকৰে।
উত্তৰঃ
অপসাৰণ কৰা ধাতু: মেগনেছিয়াম (Mg) আৰু এলুমিনিয়াম (Al) ।
অপসাৰণ নকৰা ধাতু: কপাৰ (Cu) আৰু ছিলভাৰ (Ag) ।
8. M ধাতুৰ বৈদ্যুতিক শোধনৰ বেলিকা এন'ড, কেথ'ড আৰু বিদ্যুৎবিশ্লেষ্য কি ল'ব লাগিব?
উত্তৰঃ
এন'ড: অশুদ্ধ M ধাতুৰ এটা ডাঠ পাত ।
কেথ'ড: বিশুদ্ধ M ধাতুৰ এটা পাতল পাত ।
বিদ্যুৎবিশ্লেষ্য: M ধাতুৰ যিকোনো এটা দ্ৰৱণীয় লৱণৰ দ্ৰৱ ।
9. প্রত্যুষে সৰু চামুচ এখনত ছালফাৰ গুড়ি লৈ উত্তাপিত কৰিলে। উদ্ভৱ হোৱা গেছটো তেওঁ চিত্ৰত দেখুৱা ধৰণে এটা পৰীক্ষানলী ওভোটাকৈ ধৰি সংগ্ৰহ কৰিলে।
(a)(i) শুষ্ক লিটমাচ কাগজৰ লগত
উত্তৰঃশুষ্ক লিটমাচ কোনো পৰিৱৰ্তন নহয় ।
(ii) সিক্ত লিটমাচ কাগজৰ লগত গেছটোৰ বিক্রিয়া কেনে হ'ব?
উত্তৰঃসিক্ত ৰঙা হ’ব, কাৰণ অধাতৱ অক্সাইড পানীত দ্ৰৱীভূত হ’লে আম্লিক হয় ।
(b) ইয়াত বিক্ৰিয়াটোৰ সন্তুলিত সমীকৰণ লিখা।
উত্তৰঃ ইয়াত বিক্ৰিয়াটোৰ সন্তুলিত সমীকৰণ-
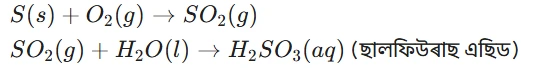
10. লোত মামৰ ধৰা ৰোধ কৰিবলৈ দুটা উপায় বর্ণনা কৰা।
উত্তৰঃলোত মামৰ ধৰা ৰোধ কৰিবলৈ দুটা উপায়-
১. ৰং কৰি বা তেল/গ্ৰীজ সানি ।
২. দস্তালেপন বা গেলভানাইজেছন কৰি (যিংকৰ প্ৰলেপ দি)
11. অক্সিজেনৰ লগত বিক্রিয়া কৰি অধাতুবিলাকে কেনে অক্সাইড উৎপন্ন কৰে?
উত্তৰঃঅধাতুবিলাকে অক্সিজেনৰ লগত বিক্ৰিয়া কৰি সাধাৰণতে আম্লিক অক্সাইড উৎপন্ন কৰে ।
১২. কাৰণ দৰ্শোৱা:
(a) গহনা তৈয়াৰ কৰিবলৈ প্লেটিনাম, গ'ল্ড আৰু ছিলভাৰ ব্যৱহাৰ কৰা হয়।
উত্তৰঃ সক্ৰিয়তা শ্ৰেণীৰ একেবাৰে তলত থকাৰ বাবে প্লেটিনাম, গ'ল্ড আৰু ছিলভাৰ অতিকৈ নিষ্ক্ৰিয় ধাতু । এই ধাতুবোৰ বায়ু, পানী বা এছিডৰ সংস্পৰ্শত সহজে ক্ষয় নহয় আৰু ইয়াৰ উজ্জ্বলতা বা ধাতৱ দ্যুতি বহু দিনলৈ অটুট থাকে ।ইয়াৰ উপৰি এই ধাতুবোৰ যথেষ্ট নমনীয় (ductile) আৰু ঘাতসহনশীল (malleable), যাৰ বাবে গহনাৰ বিভিন্ন জটিল নক্সা তৈয়াৰ কৰাটো সহজ হয় ।
(b) ছ'ডিয়াম, পটাছিয়াম আৰু লিথিয়াম ধাতু তেলত ডুবাই ৰখা হয়।
উত্তৰঃ ছ'ডিয়াম, পটাছিয়াম আৰু লিথিয়াম অতিকৈ সক্ৰিয় ধাতু (alkali metals) ।এই ধাতুবোৰে অক্সিজেন আৰু পানীৰ সংস্পৰ্শত ইমান প্ৰৱণতাৰে বিক্ৰিয়া কৰে যে মুক্ত বায়ুত ৰাখিলে বা পানীৰ সংস্পৰ্শলৈ আহিলে লগে লগে জুই জ্বলি উঠে । এনেধৰণৰ দুৰ্ঘটনা ৰোধ কৰিবলৈ আৰু ধাতুবোৰক বায়ুৰ অক্সিজেন বা জলীয় বাষ্পৰ পৰা আঁতৰাই ৰাখিবলৈ কেৰাচিন তেলত ডুবাই ৰখা হয় ।
(c) এলুমিনিয়াম যথেষ্ট সক্রিয় ধাতু তথাপি ইয়াক ৰন্ধনত ব্যৱহাৰ কৰা বৰ্তন তৈয়াৰ কৰিবলৈ ব্যৱহাৰ কৰা হয়।
উত্তৰঃ এলুমিনিয়াম যথেষ্ট সক্ৰিয় হ’লেও বায়ুৰ সংস্পৰ্শত ইয়াৰ পৃষ্ঠভাগত এলুমিনিয়াম অক্সাইডৰ (Al2O3) এটা অতি পাতল আৰু সুস্থিৰ আৱৰণৰ সৃষ্টি হয় ।এই অক্সাইডৰ তৰপটোৱে এলুমিনিয়ামক অধিক ক্ষয় যোৱাৰ পৰা ৰক্ষা কৰে । ইয়াৰ উপৰি এলুমিনিয়াম তাপৰ অতি সুপৰিবাহী আৰু ই ওজনত যথেষ্ট পাতল, যাৰ বাবে ইয়াক ৰন্ধন কাৰ্যত ব্যৱহাৰ কৰা বৰ্তন তৈয়াৰ কৰিবলৈ উত্তম বুলি গণ্য কৰা হয় ।
(d) ধাতু নিষ্কাশনৰ সময়ত কার্বনেট আৰু ছালফাইড আকৰ অক্সাইডলৈ ৰূপান্তৰ কৰা হয়।
উত্তৰঃধাতু নিষ্কাশনৰ সময়ত কাৰ্বনেট বা ছালফাইড আকৰৰ তুলনাত অক্সাইড আকৰৰ পৰা ধাতু আহৰণ কৰাটো যথেষ্ট সহজ ।অক্সাইড আকৰৰ পৰা উপযুক্ত বিজাৰক (যেনে- কাৰ্বন) ব্যৱহাৰ কৰি ধাতুলৈ বিজাৰিত কৰা প্ৰক্ৰিয়াটো কাৰ্বনেট বা ছালফাইড আকৰৰ নিষ্কাশন প্ৰক্ৰিয়াতকৈ অধিক লাভজনক ।সেয়েহে, বিজাৰণ প্ৰক্ৰিয়াৰ আৰম্ভণিতে দগ্ধীকৰণ (calcination) বা তাপজাৰণ (roasting) পদ্ধতিৰ সহায়ত কাৰ্বনেট আৰু ছালফাইড আকৰবোৰ ধাতৱ অক্সাইডলৈ ৰূপান্তৰ কৰি লোৱা হয় ।
13. চেকা লগা কপাৰৰ পাত্ৰ নেমু বা তেতেলী (tamarind) ৰসেৰে পৰিষ্কাৰ কৰা দেখিছানে? পাত্ৰবিলাক পৰিষ্কাৰ কৰিবলৈ টেঙাজাতীয় বস্তু কিয় ব্যৱহাৰ কৰে?
উত্তৰঃকপাৰে বতাহত থকা সেমেকা কাৰ্বন ডাইক্সাইডৰ সৈতে বিক্ৰিয়া কৰাৰ ফলত ইয়াৰ পৃষ্ঠত ক্ষাৰকীয় কপাৰ কাৰ্বনেটৰ এটা সেউজীয়া আৱৰণ পৰে । নেমু বা তেতেলীৰ দৰে টেঙা বস্তুত জৈৱিক অম্ল (Acid) থাকে । এই অম্লই ক্ষাৰকীয় কপাৰ কাৰ্বনেটৰ তৰপটোৰ সৈতে বিক্ৰিয়া কৰি তাক দ্ৰৱীভূত কৰে আৰু পাত্ৰটোৰ পৰা আঁতৰাই পেলায় । ফলস্বৰূপে, কপাৰৰ পাত্ৰটো পুনৰ পৰিষ্কাৰ আৰু উজ্জ্বল হৈ পৰে ।
14. ৰাসায়নিক ধৰ্মৰ ভিত্তিত ধাতু আৰু অধাতুৰ পাৰ্থক্য লিখা?
উত্তৰঃ
| বৈশিষ্ট্য | ধাতু (Metals) | অধাতু (Non-metals) |
| আয়ন গঠন | ধাতুৱে ইলেক্ট্ৰন এৰি দি ধনাত্মক আয়ন (cation) গঠন কৰে। | অধাতুৱে ইলেক্ট্ৰন গ্ৰহণ কৰি ঋণাত্মক আয়ন (anion) গঠন কৰে। |
| অক্সাইডৰ প্ৰকৃতি | ধাতুৱে অক্সিজেনৰ লগত বিক্ৰিয়া কৰি ক্ষাৰকীয় অক্সাইড উৎপন্ন কৰে। | অধাতুৱে অক্সিজেনৰ লগত বিক্ৰিয়া কৰি সাধাৰণতে আম্লিক অক্সাইড উৎপন্ন কৰে। |
| এছিডৰ লগত বিক্ৰিয়া | ধাতুবোৰে লঘু এছিডৰ লগত বিক্ৰিয়া কৰি হাইড্ৰ’জেন গেছ উৎপন্ন কৰে। | অধাতুবোৰে সাধাৰণতে লঘু এছিডৰ লগত বিক্ৰিয়া নকৰে। |
15. এজন ভণ্ড মানুহ স্বৰ্ণকাৰৰ ভাও ধৰি ঘৰে ঘৰে ঘূৰি ফুৰিছিল। তেওঁ ম্লান পৰি যোৱা অলঙ্কাৰৰ চিকমিকনি পুনৰ ঘূৰাই অনাৰ প্ৰতিশ্রুতি দি ফুৰিছিল। এগৰাকী মহিলাই কোনো সন্দেহ নকৰি হাতৰ খাৰুযোৰ খুলি তেওঁক দিছিল। মানুহজনে খাৰুযোৰ এটা বিশেষ দ্ৰাৱকত ডুবাই ধৰিছিল। খাৰুযোৰ নতুনৰ লেখিয়াকৈ উজ্জ্বল হৈ পৰিছিল; পিছে খাৰুযোৰৰ ওজন বহুখিনি কমি গৈছিল। মহিলাগৰাকী অপ্রস্তুত হৈ পৰিছিল আৰু অনর্থক বাকবিতণ্ডাৰ মূৰকত মানুহজন সেই ঠাইৰ পৰা পলাইছিল। মানুহজনে ব্যৱহাৰ কৰা দ্ৰাৱকটো কি আছিলে অনুমান কৰি কব পাৰিবা নে?
উত্তৰঃ মানুহজনে ব্যৱহাৰ কৰা বিশেষ দ্ৰাৱকটো আছিল অম্লৰাজ (Aqua Regia)।
কাৰণ: অম্লৰাজ হ’ল গাঢ় হাইড্ৰ’ক্ল’ৰিক এছিড (HCl) আৰু গাঢ় নাইট্ৰিক এছিডৰ (HNO3) এক ৩:১ অনুপাতৰ মিশ্ৰণ। যদিও এই এছিড দুটাই অকলে সোণ দ্ৰৱীভূত কৰিব নোৱাৰে, অম্লৰাজে সোণ দ্ৰৱীভূত কৰিব পাৰে। যেতিয়া মহিলাগৰাকীৰ সোণৰ খাৰুযোৰ এই দ্ৰাৱকত ডুবাই দিয়া হৈছিল, খাৰুৰ ওপৰৰ ম্লান পৰি যোৱা সোণৰ তৰপটো দ্ৰৱীভূত হৈ গৈছিল। ইয়াৰ ফলত ভিতৰৰ উজ্জ্বল সোণৰ তৰপটো ওলাই পৰিছিল আৰু খাৰুযোৰ নতুনৰ দৰে জিলিকি উঠিছিল, কিন্তু সোণ দ্ৰৱীভূত হোৱাৰ বাবে ইয়াৰ ওজন বহুখিনি কমি গৈছিল।
16. গৰম পানীৰ জলাধাৰ (hot water tanks) তৈয়াৰ কৰিবলৈ কপাৰ ব্যৱহাৰ কৰা হয়। কিন্তু ষ্টিল (আইৰনৰ সংকৰ ধাতু) ব্যৱহাৰ কৰা নহয়। কিয়?
উত্তৰঃ গৰম পানীৰ জলাধাৰ তৈয়াৰ কৰিবলৈ ষ্টিলৰ পৰিৱৰ্তে কপাৰ ব্যৱহাৰ কৰাৰ মূল কাৰণবোৰ হ’ল:
পানীৰ লগত বিক্ৰিয়া: কপাৰে ঠাণ্ডা পানী, গৰম পানী বা আনকি জলীয় বাষ্পৰ লগতো কোনো বিক্ৰিয়া নকৰে। আনহাতে, ষ্টিলত থকা আইৰনে (লো) জলীয় বাষ্পৰ লগত বিক্ৰিয়া কৰি আইৰন অক্সাইড গঠন কৰে, যাৰ ফলত জলাধাৰটো লাহে লাহে ক্ষয় হ’ব পাৰে।
তাপৰ পৰিবাহিতা: কপাৰ তাপৰ অতি সুপৰিবাহী। ই ষ্টিলতকৈ বহুত খৰকৈ পানী গৰম কৰাত সহায় কৰে।
ক্ষয়প্ৰতিৰোধ ক্ষমতা: কপাৰত মামৰ নধৰে, কিন্তু ষ্টিলত (যদিহে ই উচ্চ মানৰ ষ্টেইনলেচ ষ্টিল নহয়) সেমেকা বায়ু আৰু পানীৰ সংস্পৰ্শত মামৰ ধৰাৰ সম্ভাৱনা থাকে।